-
临床流行病学显示,终末期肾脏病患者发生房颤的风险是一般人群的10倍[1]。口服抗凝剂是预防房颤血栓形成的重要治疗方法,但现有口服抗凝剂缺乏针对终末期肾脏病患者的临床研究,其安全性和有效性并不确切[2-3]。阿哌沙班是一种新型口服Xa因子的抑制剂,广泛应用于预防和治疗血栓形成。研究显示,阿哌沙班可降低肾病合并房颤患者的大出血、血栓栓塞和死亡风险,为此类患者提供新的抗凝药物选择[3]。但阿哌沙班缺少在终末期肾脏病患者(血肌酐清除率<15 ml/min)中使用的临床资料,且目前阿哌沙班肠道吸收部位尚不明确,其吸收的影响因素也不清楚,因而,一定程度上限制了其应用。本实验拟通过探究阿哌沙班在肾衰大鼠肠道内的吸收部位、吸收机制以及P糖蛋白抑制剂对其肠道吸收的影响,以便为阿哌沙班在终末期肾脏病患者中使用提供一定的参考依据。
-
岛津LC-2030 Plus高效液相色谱仪、AUW120D电子天平(日本岛津公司);UVF超纯水器(上海和泰仪器有限公司);超声清洗仪(深圳市洁盟清洗设备有限公司);Hei-Tec磁力搅拌器(德国海道尔夫);SHZ-D循环水式真空泵(巩义市英峪予华仪器厂)。
-
阿哌沙班原料药(武汉嘉叶生物科技有限公司);十二烷基硫酸钠(南京化学试剂有限公司);氯化钠、氯化钾、碳酸氢钠、二水合盐酸二氢钠、氯化镁、氯化钙、葡萄糖、乙酸铵(上海国药集团);甲醇(上海星可高纯溶剂有限公司);纯净水(杭州娃哈哈股份有限公司)。
-
SD雄性大鼠,230~250 g,购自上海斯莱克实验动物有限公司,动物许可证号:SCXK(沪)2017-0005。动物自由饮水、进食,环境温度22~25 ℃,相对湿度60%,光照时间8:00—18:00。所有动物实验均符合实验动物伦理学要求。
-
精确称取NaCl 7.8 g、KCl 0.35 g、MgCl2·6H2O 0.02 g、NaH2P04 0.32 g、NaHCO3 1.37 g,用超纯水溶解后加入0.37 g CaCl2 至溶解完全,临用前加入葡萄糖1.4 g,转移至1000 ml容量瓶中定容至刻度,调节pH至7.4。
-
精确称取9 mg阿哌沙班原料药置于容量瓶中,加入3 % SDS,定容至100ml,作为阿哌沙班储备液备用。
-
分别取0.5、1.0、4.0ml阿哌沙班储备液至100 ml容量瓶中,加入K-R营养液,超声溶解后定容至100ml,配置成的阿哌沙班溶液浓度分别为0.45、0.90、3.60 μg/ml。
-
精确称取0.5g的盐酸维拉帕米置于100 ml容量瓶中,加入超纯水溶解配制成浓度为5 mg/ml的盐酸维拉帕米储备溶液。分别取1 ml盐酸维拉帕米储备溶液和1 ml阿哌沙班储备溶液置100ml容量瓶,配制成含盐酸维拉帕米浓度为50 μg/ml、阿哌沙班浓度为0.9 μg/ml的供试品溶液。
-
色谱柱:Gemini 5u C18 110A色谱柱(4.6 mm×250 mm,5 μm);流动相:A相为甲醇,B相为10 mmol/L醋酸胺溶液;柱温:30 ℃;流速:1.0 ml/min;进样量:10 μl。
-
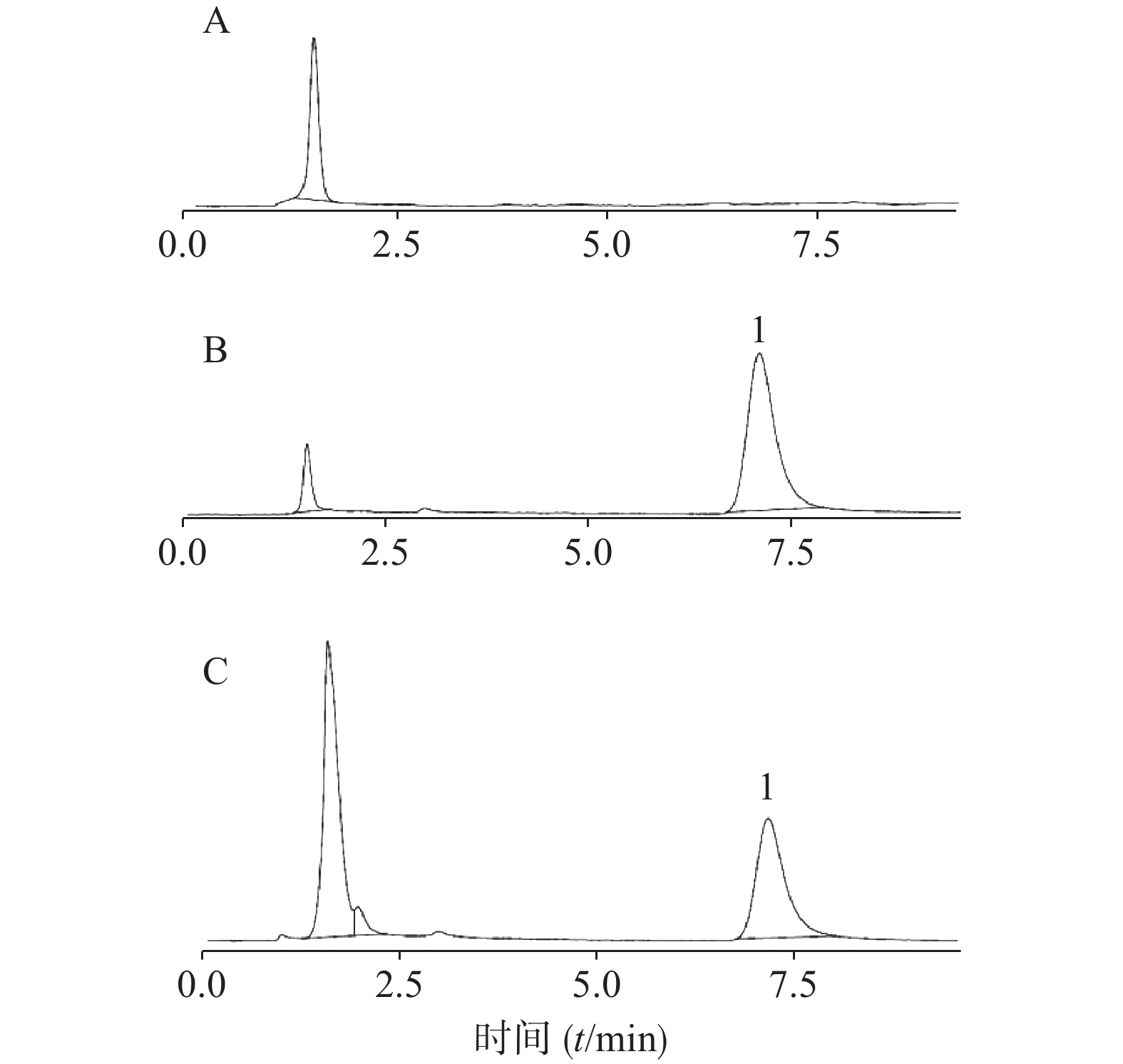
分别取空白K-R溶液、阿哌沙班K-R溶液以及阿哌沙班K-R回流收集液,2000 r/min离心5 min后取上清液10 μl,按照“2.2.1”项下色谱条件进样分析[4-5]。结果见图1。实验结果表明,肠灌流液中阿哌沙班峰形良好,保留时间约为7 min,空白K-R溶液及空白肠灌流液对其无干扰,专属性良好。
-
精密量取阿哌沙班标准储备液用K-R溶液配制系列标准溶液,各取1 ml加入0.5 ml甲醇,离心后取上清液,按照“2.2.1”项下方法进样分析。线性回归分析结果表明阿哌沙班在0.36-4.5 µg/ml范围内线性关系良好。
-
精密量取阿哌沙班标准储备液用K-R溶液配制浓度呈0.45、0.9、3.6 μg/ml的阿哌沙班供试品溶液,各取1 ml加入0.5 ml甲醇,离心后取上清液,按照“2.2.1”项下方法进样分析,计算阿哌沙班在低、中、高浓度溶液中的回收率。低、中、高浓度溶液中阿哌沙班平均回收率分别为97.39 %、98.91 %、99.92 %,RSD分别为1.94 %、1.88 %、1.25 %,结果表明本方法准确度良好。
-
精密量取阿哌沙班标准储备液用K-R溶液配制浓度为0.45、0.9、3.6μg/ml的阿哌沙班供试品溶液,置于37 ℃水浴3 h,考察药物在K-R液中的稳定性。结果0.45、0.9、3.6 µg/ml的阿哌沙班供试液的 RSD 分别为 0.51 %、1.65 %、0.50%,表明3 h内阿哌沙班的稳定性良好。
-
雄性SD大鼠适应性饲养1周后按剂量40 mg/kg腹腔注射1%戊巴比妥钠,待麻醉成功后,取仰卧位固定,常规消毒,沿左腹旁肾脏位置切开皮肤并逐层分离皮下组织进入腹腔,暴露左侧肾脏,切开上、下极的包膜,采用针形电烧灼器分别在左肾上、下极电凝肾脏表面,逐层缝合肌层和皮肤,关闭腹腔。2周后,沿右腹旁肾脏位置处切口切开皮肤,逐层分离皮下组织进入腹腔,暴露右侧肾脏,用丝线结扎右肾肾门,切除右肾。
-
取慢性肾功能衰竭大鼠,禁食12 h,期间自由饮水,按剂量40 mg/kg 腹腔注射1%戊巴比妥钠,待麻醉成功后,取仰卧位固定,常规消毒皮肤。沿腹中线取长约3 cm纵行手术切口,分别在十二指肠、空肠、回肠、结肠处各取间距约为10 cm两个微小切口,分别在两切口处置入无菌引流管,并用丝线固定。取预热至37 ℃的生理盐水冲洗肠道内容物,直至澄清液体,引流管连接恒流泵,以2.0 ml/min的起始流速将浓度为0.9 μg/ml的阿哌沙班溶液泵入肠段,待肠段内药液充满后将流速降低至0.2 ml/min,此后按15 min/次的频率收集肠回流液,计算肠回流液的质量减少量及15 min内收集到的流出液体的质量,并测定收集液中药物浓度。实验持续时间2 h。样品采集完后处死大鼠,剪下所研究的肠段,将其平铺,测量其长度以及横截面半径。
-
采用质量法对回流液流入和流出体积进行校正。按下式计算吸收速率常数(Ka)和表观渗透系数(Papp):
$$ K_{a}=(1-C_{out}V_{out}/C_{in}V_{in})v/\text{π}r^{2}L $$ $$ P_{app}=-v ln(C_{out}V_{out}/C_{in}V_{in})/2\text{π}rL $$ 式中Vin和Vout分别为灌入和收集的回流液体积(ml),Cin、Cout分别为进口和出口处回流液中药物的质量浓度(μg/ml),v为灌流速度(ml/min),r为被灌流肠段的横截面半径(cm),L为被灌流肠段的长度(cm)。
-
根据测定收集液中阿哌沙班浓度,计算不同肠段中阿哌沙班Ka和Papp,结果发现空肠对阿哌沙班的吸收速率最快,结肠段最慢,结果具有统计学意义。各肠段间的阿哌沙班表观吸收系数未见明显异常。如表1所示。
表 1 不同肠段药物吸收速率常数和表观吸收系数(n=6)
肠段 Ka×10−2/min Papp×10−4(cm/s) 十二指肠 1.43±0.18# 0.17±0.6 空肠 1.80±0.27*# 0.24±0.03 回肠 1.35±0.24# 0.16±0.03 结肠 0.87±0.18 0.14±0.05 注: #P<0.05,与结肠比较;*P<0.05,与回肠比较 -
配制浓度分别为0.45、0.9、3.6 μg/ml的阿哌沙班灌流液,按“2.3.2”项下操作流程选取肾衰大鼠回肠进行灌流,测定灌流液中阿哌沙班的浓度,计算药物Ka和Papp。结果显示,在回肠段,阿哌沙班药物浓度越高,肠道对其吸收速率和表观吸收系数越低(P<0.05),如表2所示。
表 2 回肠不同浓度药物吸收速率常数和表观吸收系数(n=6)
浓度(μg/ml) Ka×10−2/min Papp×10−4(cm/s) 0.45 1.67±0.38# 0.27±0.05# 0.90 1.35±0.24 0.16±0.03 3.60 0.81±0.18 0.13±0.03 注: #P<0.05,与高浓度组比较 -
按“2.1.4”项下方法配制含盐酸维拉帕米的阿哌沙班灌流液,按“2.3.2”项下操作流程选取大鼠空肠及回肠进行灌流,测定灌流液中阿哌沙班的浓度,计算药物Ka和Papp,研究P-gp 外排作用对阿哌沙班在空肠和回肠段的吸收特性影响。结果显示,加入维拉帕米后,阿哌沙班的Ka和Papp的值均增加,提示阿哌沙班是 P-gp 的底物,P-gp抑制剂显著促进阿哌沙班的肠吸收,如表3所示。
表 3 P-gp抑制剂对阿哌沙班在空肠和回肠段吸收特性的影响(n=6)
药物组别 空肠 回肠 Ka×10−2
/minPapp×10−4
(cm/s)Ka×10−2
/minPapp×10−4
(cm/s)阿哌沙班 1.80±0.27 0.24±0.03 1.35±0.24 0.16±0.03 阿哌沙班+维拉帕米 2.97±0.44# 0.53±0.12# 1.89±0.51* 0.31±0.04 注: # P<0.05,空肠段与阿哌沙班单药组比较;*P<0.05,回肠段与阿哌沙班单药组比较 -
阿哌沙班是新型口服、高效、高选择性的Xa因子抑制剂,自2013年上市以来,随着应用的推广,阿哌沙班适应证由早期的关节置换术后预防静脉血栓形成逐渐拓展为广泛的预防和治疗血栓的形成[6-10]。慢性肾脏病是临床常见病和多发病[11]。研究显示,相对于健康人群,终末期肾脏病患者发生房颤的风险增加10倍,严重危及终末期肾脏病患者的生命安全[1]。房颤是临床最常见的心律失常疾病,其极易诱发血栓形成,抗凝治疗是房颤病人预防血栓形成及栓塞的必要治疗手段[12]。但目前临床上常见的口服抗凝剂均缺乏针对肾脏病患者的临床研究,其安全性和有效性存疑[3,8,13]。在一项和华法林的对比中发现,相对于华法林,阿哌沙班可降低终末期肾脏病合并房颤患者的大出血、血栓栓塞和死亡风险[3]。此外有研究发现,肾功能损伤对阿哌沙班血浆浓度与抗FXa活性的关系无明显影响[14]。这也给这部分患者带来了新抗凝剂的选择。然而,对于其肠道主要吸收部位及吸收机制了解欠缺也在一定程度上限制了其临床的应用。
本研究通过比较肾衰大鼠不同肠段药物浓度的测定来推测阿哌沙班在肠道内的吸收部位及吸收机制,并通过给予P糖蛋白抑制剂来研究其对肠道吸收阿哌沙班的影响。目前研究胃肠道对药物吸收情况的方法主要分为在体实验、体外实验和体内实验三种[15]。其中在体实验又分为两种:循环灌流法和单向灌流法[15-17]。单向灌流法具有通用性好、耗时少及流速低的特点,同时显著减少了对肠道生理环境的影响,最终实验准确性高[16,18]。在本实验所测定的阿哌沙班因其溶解性低、渗透性差及难以被吸收的限制,导致肠道对酚红吸收增加,对实验结果测算校正影响大,故选用单向肠灌流法进行试验以及重量法进行校正计算[19]。
有文献报道[20],当药物的Papp小于 0.03×10−4 cm/s时表明该药物吸收较差;Papp大于0.2×10−4 cm/s时表明该药物吸收完全;而介于两者之间则为中等吸收。阿哌沙班在十二指肠、空肠、回肠、结肠的Papp值均保持约0.2×10−4 cm/s,说明阿哌沙班在各肠段均有良好吸收行为。此外,高血压是慢性肾衰患者最常见的并发症,常需使用多种降压药物联合治疗,P-gp抑制剂维拉帕米作为经典的钙通道拮抗剂广泛应用于临床降压治疗。既往研究显示,阿哌沙班和利伐沙班可被细胞色素P450 3A和P-gp所消除[21]。为进一步明确P-gp对阿哌沙班的吸收影响,本研究观察了P-gp抑制剂盐酸维拉帕米对阿哌沙班肠道吸收的影响,结果表明加入P-gp抑制剂后,阿哌沙班在空肠和回肠段Ka和Papp值均有不同程度的增加,推测阿哌沙班是P-gp的底物, P-gp抑制剂的加入有利于增加阿哌沙班的吸收程度,从而提高阿哌沙班口服生物利用度。不同浓度的阿哌沙班溶液在回肠的吸收情况不同,低浓度与高浓度之间存在显著性差异,且高浓度的Ka及Papp的值最小,表明阿哌沙班的吸收存在自身浓度抑制,其吸收机制应为主动转运。
综上所述,阿哌沙班在各肠段均有吸收;P-gp抑制剂对阿哌沙班在空肠和回肠段的吸收均有明显的促进作用,表明阿哌沙班为P-gp底物,推测其吸收机制为主动转运。本文拟通过探究阿哌沙班在肠道内的吸收部位、吸收机制以及P糖蛋白抑制剂对其肠道吸收的影响,为今后阿哌沙班的使用提供一定的参考依据。
Study on intestinal absorption characteristics of apixaban by in vivo one-way perfusion in rats with renal failure
-
摘要:
目的 研究阿哌沙班在肾衰大鼠体内的肠吸收特性,并考察P糖蛋白(P-glycoprotein,P-gp)抑制剂对阿哌沙班吸收行为的影响。 方法 选择肾衰大鼠在体单向灌流法进行肠吸收实验,建立大鼠阿哌沙班肠灌流液HPLC分析方法,以考察大鼠在体肠吸收影响因素。 结果 阿哌沙班在各肠段的吸收速率常数(Ka)存在显著性差异(P<0.05),但表观吸收系数(Papp)未见明显差异(P>0.05);大鼠回肠段的Ka和Papp值随药物浓度的增加而降低;加入 P-gp抑制剂盐酸维拉帕米(0.1 mmol/L)后,阿哌沙班在空肠和回肠段的Ka和Papp值均明显增加。 结论 阿哌沙班在各肠段均有吸收;P-gp抑制剂对阿哌沙班在空肠和回肠段的吸收均有明显的促进作用,表明阿哌沙班为P-gp底物,推测其吸收机制为主动转运。 Abstract:Objective To study the intestinal absorption characteristics of apixaban in rats with renal failure, and the effect of P-glycoprotein (P-gp) inhibitors on its absorption behavior. Methods The in vivo absorption experiment was performed in CRF rats by one-way perfusion method and the absorption factors was investigated by establishing the HPLC analysis method. Results The absorption rate constant (Ka) of apixaban in each intestinal segment was significantly different (P<0.05) with no significant difference in apparent absorption coefficient (Papp) (P>0.05). The Ka and Papp values in the rat ileum decreased with the increasing of drug concentration. After addition of P-gp inhibitor verapamil hydrochloride (0.1 mmol/L), the Ka and Papp values of apixaban in the jejunum and ileum were significantly increased. Conclusion Apixaban is absorbed in all intestinal segments. P-gp inhibitors can significantly promote the absorption of apixaban in jejunum and ileum, suggesting that apixaban is P-gp substrate and its absorption mechanism is supposed to be active transport. -
Key words:
- apixaban /
- renal failure /
- one-way perfusion /
- intestinal absorption characteristics
-
表 1 不同肠段药物吸收速率常数和表观吸收系数(n=6)
肠段 Ka×10−2/min Papp×10−4(cm/s) 十二指肠 1.43±0.18# 0.17±0.6 空肠 1.80±0.27*# 0.24±0.03 回肠 1.35±0.24# 0.16±0.03 结肠 0.87±0.18 0.14±0.05 注: #P<0.05,与结肠比较;*P<0.05,与回肠比较 表 2 回肠不同浓度药物吸收速率常数和表观吸收系数(n=6)
浓度(μg/ml) Ka×10−2/min Papp×10−4(cm/s) 0.45 1.67±0.38# 0.27±0.05# 0.90 1.35±0.24 0.16±0.03 3.60 0.81±0.18 0.13±0.03 注: #P<0.05,与高浓度组比较 表 3 P-gp抑制剂对阿哌沙班在空肠和回肠段吸收特性的影响(n=6)
药物组别 空肠 回肠 Ka×10−2
/minPapp×10−4
(cm/s)Ka×10−2
/minPapp×10−4
(cm/s)阿哌沙班 1.80±0.27 0.24±0.03 1.35±0.24 0.16±0.03 阿哌沙班+维拉帕米 2.97±0.44# 0.53±0.12# 1.89±0.51* 0.31±0.04 注: # P<0.05,空肠段与阿哌沙班单药组比较;*P<0.05,回肠段与阿哌沙班单药组比较 -
[1] STANIFER J W, POKORNEY S D, CHERTOW G M, et al. Apixaban versus warfarin in patients with atrial fibrillation and advanced chronic kidney disease[J]. Circulation,2020,141(17):1384-1392. doi: 10.1161/CIRCULATIONAHA.119.044059 [2] YAO X X, TANGRI N, GERSH B J, et al. Renal outcomes in anticoagulated patients with atrial fibrillation[J]. J Am Coll Cardiol,2017,70(21):2621-2632. doi: 10.1016/j.jacc.2017.09.1087 [3] SIONTIS K C, ZHANG X S, ECKARD A, et al. Outcomes associated with apixaban use in patients with end-stage kidney disease and atrial fibrillation in the United States[J]. Circulation,2018,138(15):1519-1529. doi: 10.1161/CIRCULATIONAHA.118.035418 [4] 张震, 孙燕. HPLC法测定阿哌沙班中的有关物质[J]. 天津药学, 2014, 26(6):9-11. doi: 10.3969/j.issn.1006-5687.2014.06.004 [5] 孙媛媛, 赵云丽, 段蒙蒙, 等. 高效液相色谱法测定阿哌沙班中的有关物质[J]. 沈阳药科大学学报, 2017, 34(1):37-42. [6] 周建光, 周颖奇. 新型口服抗凝药的特点和临床研究[J]. 临床药物治疗杂志, 2013, 11(5):8-14. doi: 10.3969/j.issn.1672-3384.2013.05.003 [7] 赵伟, 许海燕. 房颤患者脑卒中的预防: 新型抗凝药依度沙班与达比加群、利伐沙班、阿哌沙班疗效与安全性的比较[J]. 中华医学杂志, 2014, 94(33):2601. doi: 10.3760/cma.j.issn.0376-2491.2014.33.012 [8] KIMACHI M, FURUKAWA T A, KIMACHI K, et al. Direct oral anticoagulants versus warfarin for preventing stroke and systemic embolic events among atrial fibrillation patients with chronic kidney disease[J]. Cochrane Database Syst Rev,2017,11:CD011373. [9] SU X L, YAN B J, WANG L H, et al. Oral anticoagulant agents in patients with atrial fibrillation and CKD: a systematic review and pairwise network meta-analysis[J]. Am J Kidney Dis,2021,78(5):678-689.e1. doi: 10.1053/j.ajkd.2021.02.328 [10] 陆璐, 张洁, 阎昭. 阿哌沙班治疗肿瘤相关性血栓栓塞的获益与风险[J]. 天津医科大学学报, 2021, 27(3):322-325. [11] 陈崴, 张望, 余学清. 中国肾脏病临床研究现状与展望[J]. 临床肾脏病杂志, 2013, 13(1):7-9. [12] LABOVITZ A J, ROSE D Z, FRADLEY M G, et al. Early apixaban use following stroke in patients with atrial fibrillation: results of the AREST trial[J]. Stroke,2021,52(4):1164-1171. doi: 10.1161/STROKEAHA.120.030042 [13] HAREL Z, MCARTHUR E, JEYAKUMAR N, et al. The risk of acute kidney injury with oral anticoagulants in elderly adults with atrial fibrillation[J]. Clin J Am Soc Nephrol,2021,16(10):1470-1479. doi: 10.2215/CJN.05920421 [14] GUREVITZ C, GILADI E, BARSHESHET A, et al. Comparison of low and full dose apixaban versus warfarin in patients with atrial fibrillation and renal dysfunction (from a national registry)[J]. Am J Cardiol,2021,159:87-93. doi: 10.1016/j.amjcard.2021.08.022 [15] 张晓雷, 周明眉, 贾伟, 等. 在体肠灌流模型及其在中药研究中的应用[J]. 上海中医药大学学报, 2010, 24(3):87-92. [16] 莫李立, 王素军. 口服药物吸收模型的研究进展[J]. 广东药学院学报, 2011, 27(1):104-107. doi: 10.3969/j.issn.1006-8783.2011.01.026 [17] 张燕, 朱华旭, 郭立玮. 在体单向肠灌流模型研究小檗碱及其在复方配伍环境中的大鼠肠吸收特性[J]. 药学学报, 2012, 47(2):233-238. doi: 10.16438/j.0513-4870.2012.02.005 [18] 沈凯, 王景田. 药物肠吸收实验研究方法进展[J]. 中国新药杂志, 2003, 12(12):988-991. doi: 10.3321/j.issn:1003-3734.2003.12.004 [19] 王辉, 褚倩倩, 哈婧, 等. 阿哌沙班的合成新工艺[J]. 中国新药杂志, 2015, 24(11):1290-1294. [20] FAGERHOLM U, JOHANSSON M, LENNERNÄS H. Comparison between permeability coefficients in rat and human jejunum[J]. Pharm Res,1996,13(9):1336-1342. doi: 10.1023/A:1016065715308 [21] OTSUKA Y, CHOULES M P, BONATE P L, et al. Physiologically-based pharmacokinetic modeling for the prediction of a drug-drug interaction of combined effects on P-glycoprotein and cytochrome P450 3A[J]. CPT Pharmacometrics Syst Pharmacol,2020,9(11):659-669. doi: 10.1002/psp4.12562 -




 下载:
下载: